
Nafta en Mal Estado: Guía para Proteger tu Motor
¿Tu motor no arranca bien o pierde potencia? Podría ser nafta en mal estado. Aprende...
En el vasto universo de la química industrial, existen compuestos que, aunque no siempre conocidos por el gran público, son fundamentales para la creación de innumerables productos. Uno de ellos es el ácido maleico, un compuesto orgánico cuya importancia radica en su versatilidad y en las propiedades únicas que lo diferencian de su isómero, el ácido fumárico. Su origen, directamente ligado a materias primas de la industria petroquímica como el benceno y el butano, lo posiciona como un eslabón clave en la cadena de valor que transforma los recursos naturales en soluciones para la vida cotidiana. A menudo, la primera pregunta que surge sobre un compuesto es acerca de sus propiedades físicas básicas, como su punto de fusión, pero la historia del ácido maleico es mucho más profunda y fascinante.

La pregunta central sobre el ácido maleico suele ser su punto de fusión, el cual se encuentra en un rango de 131 a 139 °C. Sin embargo, este dato por sí solo no revela la complejidad de su naturaleza. Para entenderlo verdaderamente, es esencial compararlo con su contraparte geométrica, el ácido fumárico. Ambos comparten la misma fórmula química (C4H4O4), pero su disposición espacial (isómeros cis-trans) les confiere propiedades drásticamente distintas.
El ácido maleico (isómero cis) es una molécula considerablemente menos estable que el ácido fumárico (isómero trans). Esta diferencia de estabilidad se cuantifica en su calor de combustión, siendo la del ácido maleico 22,7 kJ/mol mayor. Pero, ¿a qué se deben estas diferencias tan marcadas? La respuesta está en la estructura molecular. En el ácido maleico, los dos grupos carboxilo están en el mismo lado del doble enlace carbono-carbono. Esta proximidad permite la formación de un enlace de hidrógeno intramolecular, donde un hidrógeno de un grupo carboxilo es atraído por un oxígeno del otro grupo dentro de la misma molécula. Este enlace interno consume las fuerzas que, de otro modo, se usarían para interactuar con otras moléculas, lo que explica dos de sus propiedades más notables:
En contraste, el ácido fumárico, con sus grupos carboxilo en lados opuestos, no puede formar estos enlaces de hidrógeno internos. En su lugar, utiliza todo su potencial para formar fuertes enlaces de hidrógeno intermoleculares, creando una red cristalina muy estable y robusta. Esto resulta en un punto de fusión mucho más alto (287 °C) y una solubilidad en agua muy baja.
La producción industrial del ácido maleico está intrínsecamente ligada al sector petroquímico. No se encuentra en grandes cantidades en la naturaleza, por lo que su síntesis es un proceso industrial bien establecido que parte de hidrocarburos básicos. El proceso se puede resumir en dos pasos principales:
Este proceso demuestra cómo la química transforma materias primas básicas, provenientes de yacimientos, en compuestos de alto valor añadido con aplicaciones específicas y cruciales para otras industrias.
La relación entre estos dos isómeros es uno de los ejemplos más clásicos en química orgánica para ilustrar cómo la estructura tridimensional de una molécula define su comportamiento. A continuación, se presenta una tabla comparativa para visualizar sus diferencias fundamentales.
| Característica | Ácido Maleico (Isómero Cis) | Ácido Fumárico (Isómero Trans) |
|---|---|---|
| Punto de Fusión | 131-139 °C | 287 °C (sublima) |
| Solubilidad en Agua | Alta (78 g/100 mL a 25 °C) | Muy baja (0.63 g/100 mL a 25 °C) |
| Estabilidad | Menos estable | Más estable |
| Estructura Molecular | Grupos carboxilo en el mismo lado del doble enlace | Grupos carboxilo en lados opuestos del doble enlace |
| Enlaces de Hidrógeno | Predominantemente intramoleculares | Exclusivamente intermoleculares |
La reactividad del ácido maleico lo convierte en una materia prima industrial muy valiosa. Una de sus reacciones más importantes es la isomerización para producir ácido fumárico. Aunque la rotación alrededor de un doble enlace carbono-carbono está restringida, bajo ciertas condiciones (catalizadores ácidos, luz y bromo, o tiourea) es posible convertir el ácido maleico, menos estable, en el ácido fumárico, más estable y menos soluble, lo que facilita enormemente su purificación y recolección.
Además de esta transformación, el ácido maleico es un reactivo de partida para la síntesis de otros compuestos importantes:
Finalmente, su forma ionizada, el ion maleato, y sus ésteres (conocidos genéricamente como maleatos), tienen aplicaciones específicas. Por ejemplo, el ion maleato actúa como inhibidor en ciertas reacciones bioquímicas de transaminasas, lo que le confiere interés en el campo de la investigación biológica.
El punto de fusión del ácido maleico se reporta comúnmente en un rango de 131 a 139 °C. Esta variación puede deberse a la pureza de la muestra y a las condiciones de medición.
La alta solubilidad del ácido maleico se debe a su capacidad para formar enlaces de hidrógeno con el agua. El ácido fumárico, en cambio, forma una red cristalina muy fuerte a través de enlaces de hidrógeno entre sus propias moléculas, lo que dificulta que las moléculas de agua puedan disolverlo.
Sí, es un proceso industrial y de laboratorio común llamado isomerización. Se puede lograr calentando el ácido maleico en presencia de catalizadores ácidos (como HCl) o mediante métodos fotoquímicos con bromo. La mayor estabilidad y menor solubilidad del ácido fumárico impulsan la reacción.
Su relación es directa a través de sus materias primas. Se produce a partir de anhídrido maleico, el cual se sintetiza por la oxidación de benceno o n-butano, ambos hidrocarburos obtenidos del refinamiento del petróleo y el procesamiento del gas natural.
El término “maleato” puede referirse a dos cosas: el ion maleato, que es la base conjugada del ácido maleico formada cuando pierde sus protones ácidos, o los ésteres del ácido maleico, como el maleato de dimetilo, donde los hidrógenos de los grupos carboxilo son reemplazados por otros grupos orgánicos.

¿Tu motor no arranca bien o pierde potencia? Podría ser nafta en mal estado. Aprende...
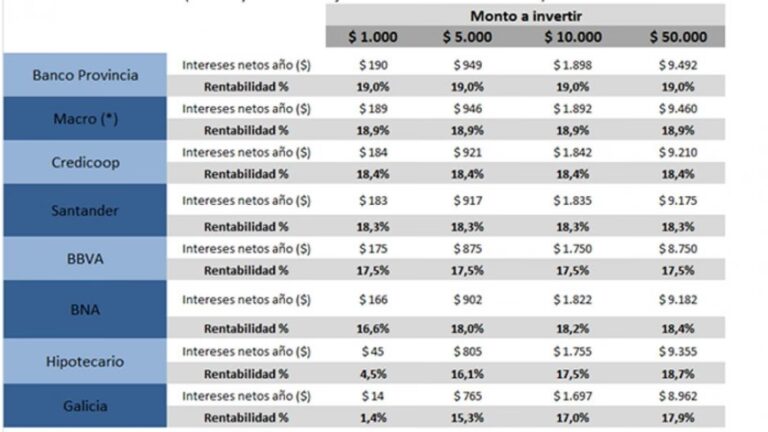
En un contexto de volatilidad, analizamos los mejores bonos argentinos para invertir. Descubre las opciones...

Descubrí la mejor ruta para llegar a Tandil en auto desde Buenos Aires. Te contamos...

Descubre con YPF los 3 pilares de la conducción defensiva: observación, anticipación y distancia. Aprende...